国产IL-4R靶点观察:千亿蓝海亟待撞线
没有人可以随随便便成功。
作为全球第二大疾病,自身免疫性疾病治疗药物的市场前景深受各方关注。
作为该领域最有潜力的靶点,白细胞介素-4受体(IL-4R)的商业化价值已经得到印证。2022年IL-4R抗体药物Dupilumab销售额高达86.81亿美元(合人民币619.63亿元)。
如此市场规模自然吸引了不少国内药企的入局。
但这个钱似乎没有那么好挣。
11月21日,康乃德(CNTB.O)宣布将用于治疗特应性皮炎的IL-4R抗体药物CBO-201的大中华区权益授权给先声药业(2096.HK),后者则预计需要付出10.25亿元以及药物上市后两位数比例的销售分成。
这一交易对价与市场期望显然有所背离,11月21日康乃德股价大跌近40%。
此番交易对价有限的核心原因或指向了CBO-201的临床数据表现并未显著优于同类药物,这导致其上市、商业化都存在一定的不确定性。
但这不影响追随者的加入。
据信风(ID:TradeWind01)不完全统计,目前A股共有智翔金泰(688443.SH)、三生国健(688336.SH)和恒瑞医药(600276.SH)3家药企的IL-4R靶点药物正在开展临床试验。
自免领域的千亿规模前景能否兑现,仍然是未知数。
一箭多雕的方向
作为一种免疫细胞因子,白细胞介素-4(IL-4)在特应性皮炎、哮喘、肿瘤和艾滋病毒感染等各种疾病的发病机制中都发挥着重要作用。
但IL-4只有与特异性受体结合才能发挥生物活性,这就像你有一把钥匙,但没有锁,那钥匙就失去了存在的意义。
“天选之子”就是特异性受体白细胞介素-4受体(IL-4R),其包括2种类型:I型受体由IL-4R亚基和c亚基组成,主要位于T细胞和NK细胞中,II型受体则由IL-4R亚基和IL-13R1亚基组成,常见于肺癌、肾癌等实体瘤中。
从组成部分就可以发现,IL-4R是共同的信号通路,因此绝大多数药企都将目光放在了IL-4R身上。
陆续有研究表明,IL-4与IL-4R结合可用于治疗特应性皮炎、哮喘等自身免疫性疾病。
自身免疫性疾病的市场前景广阔。公开数据显示,2022年全球相关的药物市场规模约为1317亿美元(合人民币9400.75亿元)。
IL-4R在自身免疫性疾病市场上的潜力已经得到印证。
2017年3月,FDA批准赛诺菲和再生元合作开发的Dupilumab上市,用于治疗中重度特应性皮炎、中重度哮喘及慢性鼻炎,其也就此成为了全球首款IL-4R抗体药物,上市当年就斩获了2.16亿欧元的销售额(合人民币16.83亿元)。
2022年,Dupilumab销售额高达86.81亿美元(合人民币619.63亿元),约为5年前的37倍。
目前,赛诺菲已将Dupilumab销售峰值目标定为130亿欧元(合人民币1012.66亿元)。
Dupilumab销售额的飙升正是IL-4R靶点巨大潜力的写照。
目前Dupilumab的适应症已经从最初的特应性皮炎、中重度哮喘及慢性鼻炎拓展至用于治疗12岁及以上体重至少40公斤人群的嗜酸性粒细胞性食管炎、疹痒性结节性瘙痒症等。
目前赛诺菲还在开展Dupilumab用于治疗慢性阻塞性肺疾病的临床试验,已进入3期试验。
3期临床数据显示,与安慰剂相比,Dupilumab在52周内可减少患者慢性阻塞性肺疾病症状30%的恶化。
“Dupilumab是第一个也是唯一一个能够显著降低COPD(慢性阻塞性肺疾病)中度或重度急性加重(呼吸道症状快速和急性恶化)的临床意义和高度显著降低(30%),同时还显著改善肺功能和生活质量的生物制剂和慢性阻塞性肺病 (COPD) 呼吸道症状。”赛诺菲指出。
慢性阻塞性肺疾病治疗药物同样前景广阔。
公开数据显示,2031年慢性阻塞性肺疾病适应治疗药物全球市场规模或可达到300亿美元(合人民币2142.48亿元)。
当头一棒
Dupilumab所取得的巨大成功让中国药企垂涎不已,许多药企正在奔向IL-4R靶点。
虽然珠玉在前,但中国IL-4R抗体药物的“吸金”能力似乎并未达到市场预期。
目前国内药企进展较快的是康乃德、康诺亚(2162.HK)。
康乃德官网显示,目前其用于治疗特应性皮炎的IL-4R抗体药物“CBO-201”在中国已进入3期临床试验。
11月21日,康乃德宣布将CBO-201的大中华区权益授权给先声药业(2096.HK)。后者则需要付出1.5亿元的预付款、8.75亿元里程碑的代价,以及两位数比例的销售分成。
此消息一出,康乃德和先声药业的股价走势呈现“冰火两重天”。
先声药业微涨2.03%,但康乃德股价大跌近39%。
究其原因,CBO-201的商业化权益或许与投资者的预期“相去甚远”。
市场期待在于,作为国内进展较快的一款IL-4R抗体药物,CBO-201的市场前景是“星辰大海”,哪怕其无法完全复制Dupilumab的成功,但至少先期的商业化权益或许不止于10亿元。
事实上,从康乃德最新披露的临床数据情况来看,CBO-201的52周疗效已较16周有了较大程度的改善。
52周的数据显示,每周给药2次的方案中,76%的患者可以保持IGA 0/1(注:皮损完全清除或基本清除)且较基线下降2分;同样的给药方案下,16周数据显示只有30.3%的患者可以保持IGA 0/1且较基线下降2分。(注:均是参照安慰剂组,下同)
但16周数据表现较Dupilumab没有优势可言,成为了一大隐忧。
Dupilumab 3期临床试验显示,每周给药2次的方案中,37%成人患者保持IGA 0/且较基线下降2分,高于CBO-201。
这不只是康乃德要面临的唯一烦恼。
此次交易让康乃德在美股市场的地位也变得岌岌可危。
11月22日收盘,康乃德的股价只有1.24美元/股。根据纳斯达克上市规则,若连续30个交易日股价低于1美元,则将收到“退市”警告。
52周的数据表现或许是先声药业此番愿意“出手”引进的重要原因。
从表面来看,这笔交易的定价相对于自身免疫性疾病的广阔市场来说并不算高价,但CBO-201是否有望在国内顺利上市仍然具有较大的不确定性,这对先声药业来说也是一场赌博。
一方面,仅从安慰剂对照组的情况来看,CBO-201的16周数据表现并未优于Dupilumab。
作为Dupilumab的后来者,CBO-201的疗效以及后期的安全性试验都需要更多的数据印证。
另一方面,康乃德并不是国内IL-4R抗体药物研发企业中的“领头羊”,后续竞争难度或将逐步加大。
目前唯一一款已进入3期注册性临床试验的IL-4R抗体国产药物源自康诺亚。
今年10月,康诺亚公布的3期注册临床数据显示,16周且每周给药2次的方案下,其IL-4R抗体药物“CM310”的IGA 0/1且较基线下降2分患者比例达到44.2%,优于康乃德。
康诺亚表示年内有望递交CM310新药上市申请。
不过,CM310的审批过程并不顺利,康诺亚本计划和Dupilumab一样采取16周的临床数据申报上市,但根据《特应性皮炎治疗药物临床试验技术指导原则》的要求,康诺亚需要将临床数据补充至52周。
追随者众
康乃德“不够给力”的授权交易,康诺亚“不算顺利”的药品审批之路,或许都在给后来者更多压力。
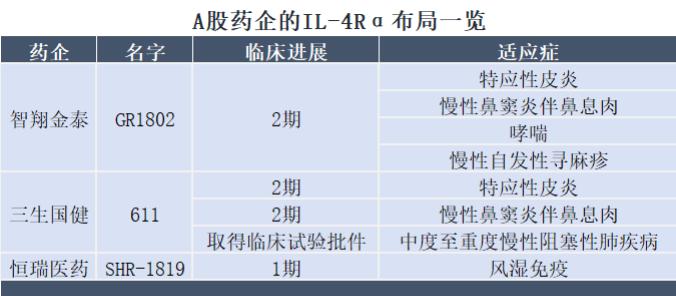
A股药企也在IL-4R靶点上有所布局。
据信风(ID:TradeWind01)不完全统计,目前A股共有智翔金泰、三生国健和恒瑞医药3家药企在IL-4R靶点上取得了临床进展。
不考虑适应症的情况下,目前整体临床进展最快的是三生国健。
今年9月,三生国健旗下用于治疗特应性皮炎的IL-4R抗体药物“611”已经达到2期临床试验的终点,或即将进入3期临床试验阶段。
对此,信风(ID:TradeWind01)11月24日致电三生国健求证目前大体的进展情况,其表示仍在与有关部门沟通临床方案。
“我们三期要等药监局通过这个临床方案之后,我们才能进行进入三期。”三生国健向信风(ID:TradeWind01)表示。
智翔金泰的进展略慢于三生国健。半年报显示,目前其IL-4R抗体药物“GR1802”用于各类自身免疫性疾病治疗的试验均处于2期。
恒瑞医药的IL-4R抗体药物“SHR-1819”则仍处于1期临床试验阶段。
尽管IL-4R抗体药物可用于治疗各类自身免疫性疾病,但从适应症布局来看,三生国健、智翔金泰都优先瞄准了特应性皮炎。
这或许与该群体的支付能力较强有关。
作为一种慢性、复发性、炎症性皮肤病,特应性皮炎会导致皮肤干燥、慢性湿疹样皮损和明显瘙痒等,会给患者带来容貌焦虑等各种精神压力,多发于婴幼儿及年轻的患者。
公开数据显示,我国的特应性皮炎患病率在婴幼儿期、1-7岁学龄前儿童、成人群体的患病率分别为30.48%、12.94%和10.6%。
“目前我国的患者估计有7000万人,这么多人饱受疾病(特应性皮炎)的折磨,而10年以上的病程的患者,一年就诊29次,平均69%的患者1个月要前往门诊1-3次,疾病负担很重。”首都医科大学北京儿童医院皮肤科医生马琳今年11月公开表示。
Dupilumab的价格可达到约3000元/支的水平,高频率的就医频率下经济负担并不算轻。
但由于患者群体较为年轻,因此整体付费意愿更强,药企选择从特应性皮炎切入或许可以更快“变现”。
与三生国健、智翔金泰不同的是,恒瑞医药切入的适应症是风湿免疫。
公开资料显示,风湿免疫类疾病具体包括类风湿性关节炎、强直性嵴柱炎、系统性红斑狼疮、原发性干燥综合征等。
风湿免疫类疾病的治疗药物在国外市场表现同样亮眼。
2022年,艾伯维(ABBV.N)旗下针对风湿免疫类疾病的修美乐销售额达到212.37 亿美元。
但修美乐在中国市场表现平平。
公开数据显示,修美乐2018年中国的样本公立医院和样本连锁药店的销售额分别仅有0.21亿元和0.15亿元,此后就再无更多数据披露。
事实上,我国风湿免疫类疾病患者数量约有500万名,群体数量并不算少。
核心原因指向了风湿免疫类疾病患者多发于老年人,这类群体的支付能力有限。
公开数据显示,修美乐初入中国市场时定价高达7600元/支,此后随着仿制药上市,市场竞争加剧,这一药物的价格才降低至600元/支左右。
恒瑞医药瞄准风湿免疫市场或意在海外,目前SHR-1819实验地位于澳洲。
谁可以复制Dupilumab的成功,市场正在拭目以待。
Reprinted from 见闻VIP,the copyright all reserved by the original author.
Disclaimer: The content above represents only the views of the author or guest. It does not represent any views or positions of FOLLOWME and does not mean that FOLLOWME agrees with its statement or description, nor does it constitute any investment advice. For all actions taken by visitors based on information provided by the FOLLOWME community, the community does not assume any form of liability unless otherwise expressly promised in writing.
FOLLOWME Trading Community Website: https://www.followme.com



Hot
No comment on record. Start new comment.